Какие бывают группы риска при беременности?
Содержание:
Значение
Различия людей по Р.-ф. могут приводить к иммунологически конфликтной беременности (см. Беременность, Несовместимость иммунологическая). В основе сенсибилизации лежит попадание в организм резус-отрицательной женщины резус-положительных эритроцитов плода, гл. обр. через сосуды плаценты.
Механизм развития резус-конфликтной беременности представляется следующим образом. Иммунные антитела, образующиеся в организме резус-отрицательной женщины, беременной резус-положительным плодом, будучи преимущественно неполными IgG, проникают через плаценту в организм плода, вызывая гемолиз эритроцитов новорожденного и повреждение его жизненно важных органов (кроветворной ткани, печени, головного мозга). Симптоматика иммунологического поражения ребенка получила название гемолитической болезни новорожденных. Вследствие обширного разрушения эритроцитов наблюдается увеличение количества билирубина, выраженная анемия с выходом в кровь большого количества эритробластов, положительная прямая проба Кумбса в результате наличия на эритроцитах плода аллоиммунных антител. Основные лечебные мероприятия по борьбе с гемолитической болезнью новорожденных сводятся к быстрейшему выведению из организма ребенка продуктов разрушения эритроцитов. Они включают в первую очередь обменные переливания резус-отрицательной крови. Развиваются и другие пути в борьбе с гемолитической болезнью новорожденных — профилактика противорезусной сенсибилизации резус-отрицательных женщин при первой беременности путем введения противорезусного гамма-глобулина.
Противорезусный гамма-глобулин приготавливают из сыворотки крови иммунного лица, содержащего антитела анти-D(DC) в титре не ниже 1 : 128—256. Введение противорезусного гамма-глобулина в дозе около 300 мг в первые 48—72 часа с момента родоразрешения предупреждает развитие сенсибилизации при следующей беременности к Р.-ф. в 90—100% случаев. Меньшую дозу противорезусного гамма-глобулина (100 мг) используют при осуществлении искусственного прерывания беременности у резус-отрицательной женщины. Механизм иммуносупрессивного действия противорезусного гамма-глобулина до конца не выяснен. Известно, что пассивное наведение у резус-отрицательной женщины противорезусного иммунитета сокращает время циркуляции в крови и разрушение макрофагами и другими клетками резус-положптельных эритроцитов плода. По-видимому, антигены Р.-ф. после соединения с антителами анти-резус теряют свою иммунизирующую активность или происходит активация Т-супрессоров (см. Иммунокомпетентные клетки).
Антигены Р.-ф
имеют важное значение в судебной медицине при проведении экспертизы по исключению отцовства (см. Отцовство спорное).
Библиография: Аграненко В. А. и Скачилова H. Н. Гемотрансфузи-онные реакции и осложнения, М., 1979; Гаврилов О. К. Пособие по транс-фузиологии, с. ИЗ, М., 1980; Доссе Ш. Иммуногематология, пер. с франц., М., 1959; Зотиков Е. А. Антигенные системы человека и гомеостаз, М., 1982; Косяков П. Н. Изоантигены и изоантитела человека в норме и патологии, М., 1974; Руководство по общей и клинической трансфузиологии, под ред. Б. В. Петровского, с. 114, 216, М., 1979; Руководство по применению крови и кровезаменителей, под ред. А. Н. Филатова, с. 86 и др., Л., 1973; Соловьева Т. Г. Резус-фактор и его значение в клинической практике, Л., 1963; Туманов А. К. и Томилин В. В. Наследственный полиморфизм изоантигенов и ферментов крови в норме и патологии человека, М., 1969; Умнова М. А. и др. Изоиммунология и вопросы гемотрансфузионных осложнений, М., 1979; Allen F. H. a. R о-s e n f i e 1 d R. F. Review of Rh serology, Haematologica, v. 6, p. 113, 1972; American hospital supply corporation, Dade division, Blood group immunology, theoretical and practical aspects, p. 47, Miami, 1976; G i b-1 e t t E. H. Genetic markers in human blood, Philadelphia, 1969; I s s i t t P. D., Pavone B. G. a. Shapiro M. Anti-Rh39 — a «new» specificity Rh system antibody, Transfusion, v. 19, p. 389, 1979; Landsteiner K. a. Wiener A.S. Agglutinable factor in human blood recognized by immune sera for rhesus blood, Proc. Soc. exp. Biol. (N. Y.), v. 43, p. 223, 1940; M о 1 1 i s о n P. L. Blood transfusion in clinical medicine, Oxford, 1979; Race R. R. a. Sanger R. Blood groups in man, Oxford, 1975; Rosen-field R. E. a. o. A review of Rh serology and presentation of a new terminology, Transfusion, v. 2, p. 287, 1962; Z m i e v s k i j С. M. Immunohematology, N. Y., 1978.
Симптомы
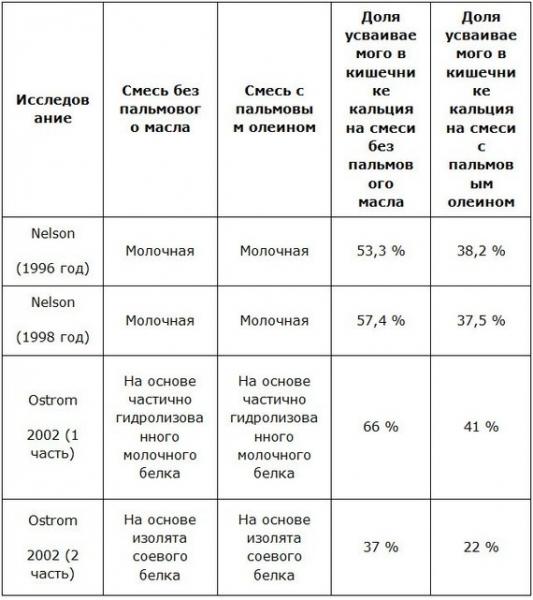
Если никаких сопутствующих заболеваний нет, то самочувствие женщины даже при резус-конфликте никак не меняется. Внешне обнаружить это отклонение нельзя. Для выявления патологии используются следующие исследования:
|
Метод диагностики |
Что показывает |
|
Анализ на резус-конфликт |
Увеличение содержания антител в крови. Опасными являются резкое повышение или скачкообразное изменение их титра. |
|
УЗИ |
|
|
Оценка уровня билирубина в околоплодной жидкости |
Оценивает интенсивность распада эритроцитов. |
Последствия
Во время первой беременности вероятность резус-конфликта практически исключена. Это объясняется тем, что вырабатываемые иммуноглобулины IgM имеют большие размеры, из-за чего не могут проникнуть через плаценту и попасть в кровь плода.
При последующих беременностях количество таких антител увеличивается. Кроме того, уменьшается их размер, из-за чего вероятность резус-конфликта повышается. Если плод не погиб на 20–30 неделе, то после рождения развиваются следующие осложнения:
- гемолитическая болезнь новорожденных;
- вялость мышц;
- срыгивание;
- трудности при кормлении;
- детский церебральный паралич;
- увеличение живота;
- бледность или желтушность кожи, каймы губ, конъюнктивы глаз;
- постоянный пронзительный плач, беспокойство;
- опистотонус – выгибание дугой со спазмами мышц рук.
Тактика ведения беременности в зависимости от полученных результатов обследования
- В срок беременности более 34 нед при наличии у пациентки дельта ОП-450 нм в зоне III или уровня фетального гематокрита ниже 30%, а также при ультразвуковых признаках водянки плода должно быть предпринято родоразрешение.
- В гестационный срок менее 34 нед при аналогичных показателях требуется либо внутриматочная гемотрансфузия, либо родоразрешение.
Окончательное решение должно быть принято на основании оценки зрелости легких плода, данных акушерского анамнеза и нарастания уровня билирубина в амниотической жидкости и возможностей перинатальной службы. Если нет условий для проведения внутриматочных гемотрансфузий, следует провести профилактику респираторного дистресс-синдрома кортикостероидами в течение 48 ч. Родоразрешение может быть предпринято спустя 48 ч после введения первой дозы кортикостероидов. Необходимо помнить, что после введения кортикостероидов снижаются показатели дельты 459 нм, при этом врач не должен считать это признаком улучшения течения заболевания.
Если срок гестации менее 34 нед, легкие плода незрелые и есть возможность для проведения внутриматочных гемотрансфузий, то приступают к их проведению.
Методы проведения внутриматочных гемотрансфузий
Существуют 2 метода проведения внутриматочных гемотрансфузий: внутрибрюшинная — введение эритроцитной массы непосредственно в брюшную полость плода (метод в настоящее время практически не используется); внутрисосудистая — введение эритроцитной массы в вену пуповины.
Внутрисосудистая гемотрансфузия является методом выбора в связи с меньшим риском осложнений и возможностью контроля за тяжестью анемии и эффективностью лечения. Кроме того, при внутрисосудистой гемотрансфузии возможен больший интервал между трансфузиями и роды могут быть отсрочены до достижения плодом более зрелого гестационного возраста.
Внутрисосудистая гемотрансфузия
Техника. Под контролем УЗИ определяют положение плода и место пункции вены пуповины. Иглой 20-го или 22-го калибра трансабдоминально под контролем УЗИ пунктируют пупочную вену недалеко от места отхождения ее от плаценты. С целью обездвиживания плода внутрисосудисто (через пупочную вену) или внутримышечно плоду вводят миорелаксанты.
Гемотрансфузию проводят с начальной скоростью 1–2 мл/мин, постепенно доводя скорость до 10 мл/мин. До и после гемотрансфу-зии эритроцитной массы определяют гематокрит плода. Конечный гематокрит определяет адекватность гемотрансфузии. Желательный конечный гематокрит (после трансфузии) — 45%. При тяжелой анемии плода с гематокритом ниже 30% трансфузии позволяют поддерживать гематокрит на уровне, близком к нормальному для данного гестацион-ного возраста (45–50%).
Требования к эритроцитной массе: группа крови 0, резус-отрицательная, тестированная и негативная на вирус гепатита В, С, цитомегаловирус и ВИЧ, совместимая с матерью и плодом, отмытая в физиологическом растворе для сведения к минимуму риска вирусного заражения.
Интервал между трансфузиями зависит от посттрансфузионного гематокрита и составляет в среднем 2–3 нед.
Внутрисосудистая гемотрансфузия обеспечивает:
- подавление продукции фетальных эритроцитов (в ответ на меньшее количество резус-положительных клеток снижается стимуляция материнской иммунной системы);
- пролонгировать беременность до более зрелого гестационного возраста плода и предотвратить осложнения, связанные с глубокой недоношенностью.
Осложнения:
- гибель плода (в отсутствие водянки плода в 0–2% случаев, при водянке плода в 10–15% случаев);
- брадикардия у плода в 8% случаев;
- амнионит в 0,5% случаев;
- кровотечение из места пункции в 1% случаев;
- преждевременный разрыв плодных оболочек в 0,5% случаев.Оценить осложнения непросто в связи с тем, что лечению подвергаются тяжело больные плоды.
Прогрессирование или регресс водянки плода может быть прослежен при УЗИ, позволяющем определить показания для повторной трансфузии. В 60–70% случаев через 2–3 нед требуется повторная трансфузия. Амниоцентез имеет малую ценность после проведения внутриматочной гемотрансфузии, когда околоплодные воды обычно загрязнены кровью. При этом возможно ложное повышение уровня билирубина в амниотической жидкости.
Роды должны быть предприняты только тогда, когда риск, связанный с преждевременными родами, меньше риска, связанного с внутриматочной трансфузией. В типичных случаях это происходит к 34-й неделе гестации. Кесарево сечение является оптимальным методом родоразрешения при водянке и тяжелой анемии у плода, когда имеется высокий риск нарушения его состояния в родах. Во время родов должна присутствовать неонатальная бригада, имеющая в своем распоряжении кровь для заменного переливания.
Токсикозы
Токсикозы возникают в первой половине срока и проявляются диспепсическими расстройствами и нарушениями всех видов обмена.
Почти в 90% случаев ранние токсикозы первой половины беременности проявляются тошнотой и рвотой. Если беременность протекает нормально, то тошнота или рвота могут возникнуть не более 2-3 раз в течение утра, чаще на голодный желудок. Эти расстройства не требуют лечения и после 12-13 недель должны пройти сами по себе.
Токсикозом считается состояние, при котором тошнота и рвота возникают в любое время суток, независимо от приемов пищи, сопровождаются снижением аппетита, истощением, слабостью и потерей веса.
Диагноз
Предположение о возможности развития Гемолитической болезни новорождённых должно возникнуть при обследовании беременной в женской консультации. Резус-отрицательная кровь у матери и резус-положительная у отца, указания в анамнезе матери на переливание крови без учета резус-фактора должны вызвать предположение о возможности Г. б. н. у ожидаемого ребенка. Наличие отягощенного акушерского анамнеза (мертворождения, самопроизвольные выкидыши, рождение детей с Г. б. н., отставание в психическом развитии старших детей) заставляет подумать о возможности более тяжелого течения Г. б. н. у ожидаемого ребенка, т. к. последующие беременности ведут к усилению сенсибилизации у изоиммунизированных женщин.
В таких случаях можно до рождения ребенка исследовать на антитела околоплодные воды, полученные с помощью амниоцентеза (см.). Наличие неполных антител в околоплодных водах говорит о конфликте средней тяжести или тяжелом, но отрицательный результат анализа не исключает возможности развития Г. б. н.
Ранний диагноз Г. б. н. и оценка тяжести заболевания должны быть проведены сразу после рождения ребенка. Наличие резус-отрицательной крови у матери и резус-положительной крови у новорожденного (при групповой несовместимости — наличие 0(I) группы у матери и А(II) или B(III) — у ребенка) и наличие резус-антител в сыворотке крови матери указывают на возможность развития Г. б. н. Для выяснения тяжести заболевания необходимо определить титр резус-антител (при высоком титре — начиная с 1 : 16 и выше — чаще имеют место тяжелые формы заболевания ребенка). При групповой несовместимости следует учитывать наличие высокого титра иммунных а- и (3-агглютининов (см. Группы крови). Как правило, в случае тяжелого течения диагноз не вызывает затруднений даже при отсутствии анамнестических данных: околоплодные воды и родовая смазка окрашены в желтый или зеленый цвет, ребенок отечный, желтушный или бледный, увеличены печень и селезенка. В неясных случаях имеет значение клин, анализ крови новорожденного, особенно пуповинной, т. к. изменения со стороны крови при Г. б. н. выявляются значительно раньше, чем другие клин, признаки заболевания. Диагностическое значение имеет снижение гемоглобина ниже 16,6 г%, наличие в крови нормобластов и эритробластов (больше чем 10 на 100 лейкоцитов), содержание билирубина в пуповинной крови выше 3 мг% по Ван-ден-Бергу, положительная проба Кумбса (см. Кумбса реакция) при резус-конфликте (при конфликте по системе AB0 — проба Кумбса отрицательная).
Рис. 2. Таблица Полачека для определения показаний к обменному переливанию крови в соответствии с динамикой билирубина у детей в первые дни жизни при гемолитической болезни новорожденных. При содержании билирубина выше верхней кривой показано обменное переливание крови, нише нижней кривой — обменное переливание крови не показано. При содержании билирубина, соответствующем промежутку между верхней и нижней кривыми, обменное переливание крови производится в зависимости от клинических данных.
Трудно бывает поставить диагноз, если Г. б. н. вызвана другими антигенами. В таких случаях проводят исследования сыворотки крови на наличие антител и определение их титра. Ранняя диагностика Г. б. н. имеет значение для срочного проведения заменного переливания крови. Если же сразу при рождении сложно решить вопрос о тяжести Г. б. н., то можно провести оценку по таблице Полачека (К. Polacek) (рис. 2) или вычислить почасовой прирост билирубина по формуле В. А. Таболина:
Bt = (Bn2 — Bn1) / (n2-n1) мг%,
где: Bt — почасовой прирост билирубина; Bn1 — уровень билирубина при первом определении; Bn2 — уровень билирубина при втором определении; n1 — возраст ребенка в часах при первом определении билирубина; n2 — возраст ребенка в часах при втором определении билирубина.
Дифференциальный диагноз: надо исключить затянувшуюся физиологическую желтуху новорожденных (см. Желтуха, у детей), транзиторную негемолитическую гипербилирубинемию (см.), наследственные гемолитические анемии — сфероцитарную Минковского — Шоффара и несфероцитарную (см. Гемолитическая анемия, Энзимопеническая анемия), желтухи вследствие дефицита глюкуронилтрансферазы или семейную негемолитическую гипербилирубинемию с ядерной желтухой — так наз. синдром Криглера — Найярра (см. Гепатозы), желтуху и анемию при сепсисе (см.), цитомегалии (см.), токсоплазмозе (см.), врожденном сифилисе (см.) и других инфекционных заболеваниях, анемии при кровотечениях и кровоизлияниях и др.
Описание
Резус-фактор (Rh) — это антиген (белок), который находится на поверхности эритроцитов, причём наиболее иммуногенным является антиген D (RhD), присутствие которого и определяет положительный резус-фактор (Rh+). Исследование выполняется с 9 полных недель беременности, т. е. с 10 недели.Для проведения исследования необходимо предоставить копию УЗИ.
Если резус-отрицательная (Rh-) женщина беременна резус-положительным (Rh+) плодом, её иммунная система начинает вырабатывать анти-D-антитела, вызывающие разрушение эритроцитов плода. Как правило, анти-D-антитела отсутствуют при первой беременности Rh+ плодом, протекающей без осложнений, однако сенсибилизация матери возникает в процессе родов. При каждой последующей беременности или при повреждении плаценты увеличивается риск развития гемолитической болезни плода. 98% случаев гемолитической болезни новорождённых связаны именно с D-резус-антигеном. При раннем проявлении резус-конфликт может стать причиной нарушения развития плода, преждевременных родов или выкидышей.Ген RHD
Делеция гена RHD в обеих гомологичных хромосомах обуславливает отрицательный резус-фактор. Наличие гена в гомозиготном или гетерозиготном состоянии определяет положительный резус-фактор у обследуемого. В случае если резус-положительные отцы являются гетерозиготными по резус-фактору, то у резус-отрицательных матерей даже при наличии отягощённого анамнеза плод в 50% случаев будет резус-отрицательным. Таким образом, для женщин с резус-конфликтной беременностью появилась возможность проведения пренатальной диагностики с целью определения резус-фактора на ДНК плода, выделенной из ворсин хориона (10–15 недель беременности) или из амниотической жидкости при проведении амниоцентеза (24 неделя беременности).
Если результаты молекулярно-генетического анализа показывают, что плод является резус-отрицательным, то отпадает необходимость в проведении последующих инвазивных процедур, и такие пациентки исключаются из дальнейшего обследования по тяжести развития гемолитической болезни плода. Кроме того, определение гетерозиготного генотипа по резус-фактору (RHD+/RHD-) у отца даёт основание для проведения преимплантационной диагностики при наличии отягощённого акушерского анамнеза (гибель детей от гемолитической болезни) и резус-сенсибилизации у матери. В результате при ЭКО будущей матери будут перенесены только резус-отрицательные эмбрионы.
Так как антирезусную профилактику иммуноглобулином человека рекомендовано проводить на 28 неделе первой и последующих беременностей, то определение резус-фактора плода на ранних сроках является необходимым. Определение Rh- плода в 1–2 триместре беременности позволит сократить расходы на регулярное определение титра анти-D-антител и антирезусную профилактику.Показания
Беременным (Rh-)-женщинам с 12 по 27 неделю беременности, если (Rh+)-отец является гетерозиготным носителем гена RhD (Генотипирование системы RhD).Подготовка
Специальная подготовка не требуется. Рекомендуется взятие крови не ранее чем через 4 часа после последнего приема пищи.Интерпретация результатов
При отрицательном результате теста, статус плода считается с высокой вероятностью резус-отрицательным, однако рекомендуется повторять тест на более поздних сроках беременности (но не позднее 27-ой недели) для подтверждения.
Положительный результат теста считается показанием к введению антирезусного иммуноглобулина, однако вопрос о его введении должен решаться только акушером-гинекологом на основании и других методов диагностики резус-конфликта.
При отсутствии антител к Rh-фактору по результатам ИФА и положительном молекулярно-генетическом тесте, рекомендуется введение антирезусного иммуноглобулина в период от 28 недель беременности (для профилактики ГБН) и не позднее 72 часов после родов (для профилактики Rh-конфликта при следующей беременности).
Диагностируем
-
Метод магнитно-резонансной томографии (МРТ, не путать с микроволновой резонансной терапией) — послойное исследование структур тканей.
-
Позволяет увидеть внутренние структуры глазного яблока даже в случаях непрозрачности его сред, измерить толщину хрусталика и др..
-
Виды, методы гинекологических обследований.
-
Компьютерная БРД основана на факте существования энергоинформационного поля, которое состоит из электромагнитных полей органов и клеток. Есть приборы, которые позволяют изъять «плохие» электромагнитные колебания и установить точный клинический диагноз.
-
Лабораторные исследования, виды, методы, описание.
Профилактика
Главная гарантия рождения здорового малыша у женщины с отрицательным резусом – своевременное введение антирезусного иммуноглобулина – вещества, нейтрализующего резусный антиген.
Эта процедура рекомендуется в определенные периоды:
- 28-32-я неделя беременности;
- через 48 часов после аборта или выкидыша;
- в течение 72 часов после родов (если малыш резус-положительный);
- сразу после амниоцентеза или биопсии хориона;
- при первых признаках (кровянистых выделениях) угрозы прерывания беременности до 28 недель;
- при отслойке плаценты.
Такая методика позволяет снизить риск развития гемолитической болезни у плода почти в 10 раз. Однако при наличии во время беременности титра антител введение антирезусного иммуноглобулина противопоказано!
Обычно родоразрешение при резус-конфликте проводится раньше планируемого срока – такое решение принимают совместно неонатологи, акушеры и врачи пренатальной диагностики. Лечение резус-конфликта – комплексное: инфузионная терапия, фототерапия, а в тяжелых случаях заменное переливание крови. Все эти процедуры при необходимости можно провести в клинике ISIDA.
Эксперт Лариса ТАТКАЛО, акушер-гинеколог клиники ISIDA ОболоньСовременные технологии уже на 10-й неделе беременности позволяют проводить диагностику резус-фактора плода по крови матери, не прибегая к рискованным процедурам. Таким образом, профилактику резус-конфликта можно назначать своевременно и только тем, кто действительно в ней нуждается. Кроме того, с помощью молекулярно-генетического анализа можно пренатально определить наличие у плода гена RhD, что не только будет полезным при подозрении на развитие резус-конфликта, но и позволит избежать ненужного введения антирезусного иммуноглобулина.
Программа клиники ISIDAПакет наблюдения беременности «Комфорт»
В отличие от базовой программы «Моя беременность» этот пакет включает также дополнительные консультации узких специалистов и вызов кареты скорой помощи.
В программу входят:
- консультации акушера-гинеколога
- консультации врачей узких специальностей;
- лабораторные исследования;
- пренатальный скрининг;
- функциональная диагностика;
- вызов кареты скорой помощи.
(также доступны другие опции)
Открытие групп крови
Группа крови, как таковая, представляет собой набор индивидуальных антигенных характеристик эритроцитов. О том, что у каждого человека — своя группа крови, стало известно в первой четверти XX века. Одним из первооткрывателей этого биологического феномена был австрийский врач, химик, иммунолог и инфекционист, лауреат Нобелевской премии по физиологии и медицине, Карл Ландштайнер. Смешивая сыворотку крови одних людей с эритроцитами, взятыми из крови других подопытных, он обнаружил, что при некоторых сочетаниях эритроцитов и сывороток происходит, их так называемое «склеивание». Но такое слипание эритроцитов и образование сгустков было не постоянно, в других случаях при работе с кровью ничего подобного не происходило. На основании этого открытия доктор Ландштайнер разработал определение их групп по типу присутствия в составе антигенов — только А, только В, А и В или отсутствие таковых. Данное разделение позволило сделать переливание крови — рутинной медицинской практикой. Именно поэтому перед родами женщин врачи обязательно выясняют группу крови и резус-фактор у ее плода, чтобы в экстренной ситуации спасти младенца, перелив ему соответствующую плазму или кровь. И гематологи прекрасно знают, что группа крови новорожденного, например, может не совпадать ни с материнской, ни с отцовской, хотя и наследует некоторые их признаки.
Эффективность ЭКО при низком АМГ
К сожалению, при очень скудном овариальном резерве шансы забеременеть с помощью ВРТ невысоки. Одним из важнейших этапов ЭКО является стимуляция овуляции, благодаря которой потом получают несколько яйцеклеток для последующего оплодотворения. При низком АМГ на стимуляцию отзовутся мизерное количество фолликулов, а если учесть, что из полученного материала необходимо отобрать наиболее жизнеспособные яйцеклетки, то процедура теряет смысл.
Так стоит ли прибегать к ЭКО при низком АМГ? Ответить на этот вопрос может только врач. Решение принимается после получения результатов комплексного обследования, составления полной картины общего состояния организма пациентки. Если уровень АМГ ниже 1, шансы забеременеть даже с помощью ЭКО невелики, тем не менее в некоторых ситуациях доктора рекомендуют использовать искусственное оплодотворение. В случаях, когда овариальный резерв истощен критически, может быть рекомендовано ЭКО с донорской яйцеклеткой.
Таким образом, ЭКО при низком АМГ возможно. Все, что требуется от пациентки – как можно скорее обратиться к опытному специалисту. Гинекологи-репродуктологи клиники ВРТ «Дети из пробирки» в течение многих лет успешно решают проблему мужского и женского бесплодия различной этиологии. Записаться на консультацию можно по телефону либо через форму заявки на сайте.
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.
Применение амниоцентеза
Амниоцентез при беременности используется прежде всего как диагностическая процедура для выявления некоторых генетических нарушений у плода — например:
- Синдрома Дауна, характеризующегося отклонениями в умственном развитии, пороками внутренних органов и аномальными особенностями внешности;
- Синдрома Патау, для которого характерны внешние аномалии, нарушения развития ЦНС и мозга, несовместимые с жизнью (новорожденный умирает спустя несколько дней);
- Синдрома Эдвардса, сопровождающегося нарушениями в строении внутренних органов (чаще всего сердца), задержкой умственного развития, ранней смертностью (средняя продолжительность жизни таких детей — несколько месяцев);
- Синдрома Тернера, проявляющегося исключительно у девочек в виде пороков развития внутренних органов, бесплодием, низкорослостью (хотя люди с такой патологией не имеют отклонений в интеллектуальном развитии и могут вести полноценную жизнь);
- Синдрома Клайнфельтера, характерного только для мужчин и сопровождающегося удлинением конечностей, высоким расположением талии, гинекоматией, замедленным половым созреванием, атрофией яичек, бесплодием.
Помимо выявления генетических аномалий у плода, амниоцентез при беременности применяется для контроля общего развития органов и систем ребенка у женщин, входящих в группы риска.
Показаниями к амниоцентезу являются:
- Наличие у беременной женщины или ее родственников генетических аномалий;
- Возраст женщины, превышающий 35-летнюю отметку (после нее повышается риск образования в яичниках лишней 21 хромосомной пары);
- Результаты ультразвукового обследования — например, выявление увеличенного просвета между шейной костью и кожей плода, характерного для синдрома Дауна;
- Результаты биохимического скрининга — превышение нормального уровня ХГЧ или аномально низкая концентрация РАРР-А (специфического белка, содержащегося в плазме крови).
Еще одной областью использования этой методики является искусственное прерывание беременности. В этом случае с помощью пункционной иглы в амниотическую жидкость вносятся растворы препаратов, убивающих плод и способствующих его отторжению и изгнанию из матки.
На каком сроке делают амниоцентез?
Данная процедура может быть проведена на различных сроках беременности, но не ранее 10 недели после зачатия. Именно тогда происходит формирование основных систем и органов плода, поэтому амниоцентез будет эффективен в качестве диагностической процедуры. Оптимальный срок для проведения этой операции — с 15 до 20 неделю. Обусловлено это тем, что в данный период существенно уменьшается риск нанесения плоду повреждений, увеличивается объем околоплодных вод, что облегчает взятие пробы на анализ.
Оптимальный срок для амниоцентеза определяется исходя из ее целей:
- для выявления генетических нарушений плода пункция выполняется на 15 неделе;
- для проверки формирования дыхательной системы эмбриона оптимальный срок — 3 триместр;
- для определения состояния плода в случае резус-конфликта амниоцентез осуществляется в последние месяцы беременности.
Если по каким-либо медицинским причинам (зачастую это патологии плода, несовместимые с жизнью) женщине предписан аборт, то посредством проведения амниоцентеза в мочевой пузырь вводят инъекционные абортивные препараты для прерывания беременности.