Когда кишечная палочка больше не несет пользу, или как бороться с симптомами эшерихиоза
Содержание:
Вольерный кашель
Данное заболевание известно еще как инфекционный трахеобронхит – острое контагиозное заболевание собак, которое вызывается комплексом бактерий и вирусов. Они могут оказать негативное влияние не только в совокупности, но и отдельно друг от друга. Среди них вирус парагриппа, аденовирус 2 типа, реовирус, герпес собак, стрептококки, стафилококки, микоплазмы, а также бактерия Bordetella bronchiseptica.
Зараженное животное распространяет заболевание преимущественно через слюну, носовые отделения, слезную жидкость. Реже заражение происходит через мочу и кал. Поэтому основным путем заражения признан воздушно-капельный путь, контактно-бытовой реже, но он все же не исключается. Содержание нескольких животных в одном вольере, слабые гигиенические условия увеличивают риск заражения. Также в зоне опасности оказываются посетители выставок собак, или площадок с массовым выгулом питомцев, хотя риски в этом случае и снижены, но они сохраняются.
Первые симптомы заражения могут появиться уже через 1-3 дня, максимально до 10 дней. Здоровое животное на 7-10 день самостоятельно справляется с инфекцией благодаря крепкой иммунной системе. Но это в том случае, если вольерный кашель вызван вирусом, так как бактерии и микоплазмы могут присутствовать в организме дольше, соответственно и клинические симптомы будут появляться позднее. В результате заболевание может обрести хроническое течение.
Симптомы вольерного кашля
Клинические признаки вольерного кашля включают в себя:
- Сухой приступообразный кашель. Появляется спустя несколько дней после начала заболевания. Кашель является основным симптомом заболевания. Он может усиливаться при воздействии раздражителя, а со временем появляется пенистая мокрота белого цвета, которая может напоминать по внешнему виду скудные рвотные массы.
- Выделения из носа, глаз.
- Повышение температуры тела.
- Угнетенное настроение, апатичность.
Респираторные признаки со временем усиливаются, что говорит о присоединении бактериальной инфекции, и как следствие, развитии воспаления легких.
Длительность заболевания и тяжесть его течения напрямую зависят от иммунного статуса животного, количества инфекций, которые спровоцировали вольерный кашель. Хронические заболевания бронхолегочной и других органов и систем, проведение вакцинации и другие меры профилактики также влияют на степень тяжести и саму возможность заболеть, хотя и не являются при этом 100% гарантом безопасности
Однако именно меры предосторожности значительно сокращают риски и длительность заболевания при его диагностировании. Взрослая здоровая собака может переболеть данным видом кашля в течении 1-2 недель без каких-либо последствий
А вот щенки более уязвимы, так как их иммунитет слабее. Взрослые особи с хроническими заболеваниями в анамнезе рискуют получить такие осложнения, как отек легкого.
Грамотная квалифицированная помощь ветеринара – это главный аспект в лечении вольерного кашля у собак. Не стоит затягивать с визитом в ветеринарную клинику, и уже при первых признаках болезни необходимо показать питомца специалистам.
Общие принципы лечения мочевых инфекций
- Антибактериальная обработка.
- При выборе препарата и способа его применения учитывается:
- лекарственная чувствительность штамма бактерий;
- переносимость препарата пациентом;
- тяжесть инфекции;
- медицинские затраты.
- Симптоматическое лечение в зависимости от вида недуга:
- постельный режим;
- регулярное и полное опорожнение мочевого пузыря;
- обезболивающие, спазмолитики;
- прием жидкости (диурез более 1,5 л в сутки);
- отказ от нефротоксических препаратов.
Прием жидкости
Основная цель антимикробного лечения – устранение патогенных бактерий и предотвращение рецидивов ИМП. Лечебные процедуры дифференцируются в зависимости от тяжести инфекции и чувствительности бактерий к применяемым препаратам.
В настоящее время у нас есть ряд лекарств, которые особенно полезны при лечении ИМП. К ним относятся антибиотики, фторхинолоны, химиотерапевтические агенты (например, Бактрим, Уротрим, Биспетол) и растительные препараты.
Основной принцип противомикробного лечения – провести антибиотикограмму бактерий, выросших из воспаленного участка, и провести целенаправленное лечение. В случае острых инфекций с неприятными признаками, высокой температурой и общими симптомами урологи в качестве препаратов первого ряда назначают антибиотики широкого спектра действия, действующие на грамотрицательные бактерии. В этих случаях все чаще рекомендуется использование фторхинолонов.
Пациент должен сдать мочу на бактериологический анализ и антибиотикограмму перед началом лечения, а также через 2, 14, 30 дней после начала лечения. Если есть подозрение на сепсис мочи во время пика лихорадки, берется кровь на посев и антибиотикограмму, и дополнительно начинается лечение двумя антибиотиками широкого спектра действия.
Антибиотикограмма
Терапия дисбактериоза
Лечебные мероприятия по восстановлению состава микрофлоры могут потребовать продолжительного времени. Для того чтобы терапия была эффективной , необходимо обратиться к специалисту, который после ряда обследований и на основании жалоб больного сможет подобрать максимально эффективное средство от дисбактериоза.
При любом течении заболевания лечение включает в себя следующие пункты:
-
прием лекарственных препаратов, помогающих нормализовать микрофлору кишечника и восстановить баланс между полезными и патогенными микроорганизмами;
-
включение в терапию бактериофагов, которые помогают подавить рост и численность вредных бактерий, предназначенных для лечения 1 и 2 степени дисбиоза;
-
соблюдение правил питания, которое заключается в исключении группы продуктов, способствующих размножению вредных бактерий и включениепробиотических продуктов, богатых живыми полезными микроорганизмами
От того, насколько будет правильно и эффективно проведено лечение зависит дальнейшее состояние здоровье кишечника
Поскольку флора кишечника очень чувствительна к внешним раздражителям, то очень важно соблюдать все рекомендации по комплексному лечению и методам профилактики, что поможет снизить до минимума риск развития дисбиоза в будущем
Терапия дисбиоза основывается не только на тяжести течения болезни, но и причинах развития. Эффективность и исход лечения может быть только при условии комплексного подхода, который состоит из следующих восстановительных мероприятий:
-
восстановление уровня бактерий;
-
восстановление опорожнения кишечника;
-
восстановление иммунной защиты;
-
возобновление транспортировки питательных веществ, получаемых из пищи в межклеточное пространство, кровь и лимфатическую систему.
Лекарственные препараты позволяютвосстановить микрофлору кишечника, устранить неприятную симптоматику болезни, а также скорректировать иммунитет.
Наиболее эффективно восстанавливает бифидумбактерии и лактобактерии в кишечнике кисломолочный пробиотический продукт лечебно-профилактического питания бифилакт БИОТА, в котором эти бактерии находятся в живом состоянии, что позволяет им адгезироваться (прикрепляться) не стенки кишечника и эффективно размножаться ( БИФИЛАКТ БИОТА ДЛЯ ЛЕЧЕНИЯ ДИСБАКТЕРИОЗА У ВЗРОСЛЫХ)
Какие антибиотики существуют и принцип их действия
Антибиотики назначают при развитии бактериальных инфекций, которые плохо поддаются лечению. Принцип их действия — борьба с бактериями-возбудителями. Антибиотики лишают микроорганизмы возможности размножаться, либо полностью уничтожают их.
Если неизвестно, какая именно бактерия вызывает воспаление, применяют антибиотики широкого спектра — они уничтожают как плохие, так и хорошие бактерии.
Группы антибиотиков
Большинство антибиотиков можно разделить на шесть групп:
| Антибиотик | Применение |
|---|---|
| Пенициллины (пенициллин, амоксициллин) | Инфекции, в том числе кожные, грудные и инфекции мочевыводящих. путей |
| Цефалоспорины (цефалексин) | Широкий спектр инфекций, а также сепсиса и менингита. |
| Аминогликозиды (гентамицин, тобрамицин) | Серьезные инфекционные заболевания как сепсис. Используются в основном в медицинских учреждениях, так как могут вызывать серьезные побочные. реакции |
| Тетрациклины (тетрациклин, доксициклин) | Акне и розацеа. |
| Макролиды (эритромицин, кларитромицин) | Инфекции легких и грудной клетки, устойчивые к пенициллину штаммы бактерий, аллергия на пенициллин. |
| Фторхинолоны (ципрофлоксацин, левофлоксацин) | Инфекции дыхательных путей и мочевыводящих путей. Больше не используются регулярно из-за риска серьезных побочных реакций. |
Патогенность и вирулентность
Кишечные палочки — комменсалы толстого кишечника — могут вызывать гнойно-воспалительные процессы в органах и тканях при резком снижении резистентности организма.
Вирулентность К. п. проявляется в адгезивности К. п., т. е. прилипании к ворсинкам эпителия кишки, размножении в просвете тонкой и толстой кишки, пенетрации в клетки эпителия и во внутриклеточном размножении, а также в подавлении фагоцитарной активности макрофагов и полиморфно-ядерных лейкоцитов (см. Вирулентность). К. п.— возбудители колиэнтеритов у детей раннего возраста и холероподобных заболеваний у взрослых — размножаются на поверхности эпителиальных клеток кишки. К. п. — возбудители дизентериеподобных заболеваний — проникают в клетки эпителия и размножаются в них так же, как шигеллы. Проявление вирулентности К. п. зависит от дозы бактерий, проникших в кишечник человека. Вирулентность К. п. определяется в тканевых культурах, опытах на лабораторных животных при воспроизведении экспериментального колиэнтерита, пневмонии и других процессов. Пенетрационная способность устанавливается кератоконъюнктивальной пробой Шереня путем введения культуры К. п. на конъюнктиву глаза морской свинки. К. п. образует эндотоксин, связанный с ЛПС, который является частью О-антигена. Биол, активность эндотоксина выражается неодинаково у равных серогрупп К. п. Токсические свойства эндотоксина определяются целой молекулой ЛПС, поскольку один липид или полисахарид малотоксичны. Эндотоксин поражает свертывающую систему крови, вызывает феномен Швартцмана (см. Швартцмана феномен) и другие явления, обладает пирогенными, адъювантными, протективными и митогенными свойствами. В небольших дозах стимулирует, а в больших угнетает фагоцитарную реакцию.
Многие серогруппы К. п. продуцируют энтеротоксины. Более постоянно их образует Е. coli серогрупп 06, 08, 015, 075, 078, 0148 и др. Полагают, что одни серогруппы К. п. вызывают холероподобную диарею у людей, другие только у животных (поросят, телят).
К. п. продуцируют два типа энтеротоксина. Термостабильный энтеротоксин инактивируется только после кипячения в течение 30 мин., медленно диализируется через целлофан, сохраняет активность при кислых значениях pH и после обработки трипсином и проназой. Молекулярный вес 10^3 — 10^4. Антигенными свойствами не обладает. Термолабильный энтеротоксин инактивируется после 30-минутного прогревания при 60°, pH 4,0—5,0, под действием проназы и не дуализируется. Мол. вес точно не установлен. Антигенная специфичность термолабильных энтеротоксинов, продуцируемых разными серогруппами К. п., и холерогена одинакова. Они стимулируют активность аденилциклазы и вызывают накопление циклического аденозинмонофосфата (цАМФ), что приводит к нарушению секреции и развитию острой диареи.
Для обнаружения энтеротоксигенных К. п. используют их способность вызывать расширение перевязанных участков тонкой кишки кролика и образование серозно-геморрагического экссудата. Другие методы основаны на способности термолабильного энтеротоксина активировать аденилциклазу и вызывать накопление в культуре ткани (яичников китайских хомячков, щитовидной железы свиньи) цАМФ, что приводит к индукции синтеза разных метаболитов и морфологическим изменениям клеток.
Источники и передача инфекции
Имеющаяся о STEC информация относится, в основном, к серотипу O157:H7, так как с биохимической точки зрения его можно легко дифференцировать от других штаммов E. coli. Резервуаром этого патогенного микроорганизма является, в основном, крупный рогатый скот. Кроме того, значительными резервуарами считаются другие жвачные животные (такие как овцы, козы и олени), обнаруживаются и другие инфицированные млекопитающие (такие как свиньи, лошади, кролики, собаки, кошки) и птицы (такие как куры и индейки).
E. coli O157:H7 передается человеку, главным образом, в результате потребления в пищу зараженных пищевых продуктов, таких как сырые или не прошедшие достаточную тепловую обработку продукты из мясного фарша и сырое молоко. Загрязнение фекалиями воды и других пищевых продуктов, а также перекрестное загрязнение во время приготовления пищи (через продукты из говядины и другого мяса, загрязненные рабочие поверхности и кухонные принадлежности) также могут приводить к инфицированию. Примеры пищевых продуктов, явившихся причиной вспышек E. coli O157:H7, включают не прошедшие надлежащую тепловую обработку гамбургеры, копченую салями, непастеризованный свежевыжатый яблочный сок, йогурт и сыр, приготовленный из сырого молока.
Все большее число вспышек болезни связано с потреблением в пищу фруктов и овощей (включая ростки, шпинат, латук, капусту и салат), заражение которых может происходить в результате контакта с фекалиями домашних или диких животных на какой-либо стадии их выращивания или обработки. Бактерии STEC обнаруживаются также в водоемах, (таких как пруды и реки), колодцах и поилках для скота. Они могут оставаться жизнеспособными в течение нескольких месяцев в навозе и осадочных отложениях на дне поилок. Так же была зарегистрирована передача инфекции как через зараженную питьевую воду, так и через воды для рекреационного использования.
Близкие контакты людей являются одним из основных путей передачи инфекции (орально-фекальный путь заражения). Были зарегистрированы бессимптомные носители, то есть лица, у которых не проявляются клинические симптомы болезни, но которые способны инфицировать других людей. Период выделения бактерий STEC у взрослых людей длится примерно одну неделю или менее, а у детей этот период может быть более длительным. В числе значительных факторов риска инфицирования STEC отмечается также посещение ферм и других мест содержания сельскохозяйственных животных, где возможен прямой контакт с ними.
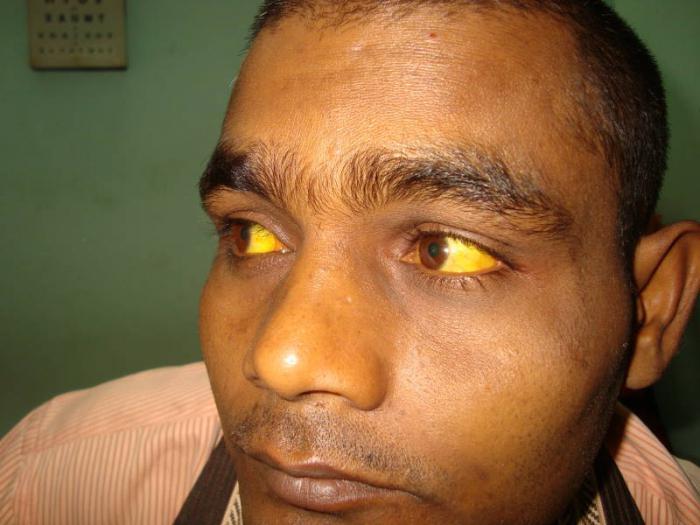
Как предотвратить эшерихиоз?
Эшерихиоз можно предотвратить, если правильно обезвреживать кал инфицированных людей, соблюдать гигиену и тщательно мыть руки с мылом. Меры профилактики, которые могут оказаться эффективными в условиях детского сада, включают разделение инфицированных и неинфицированных детей по разным группам или разрешение инфицированным детям посещать данные учреждения после 2 отрицательных культуральных исследований кала. Пастеризация молока и тщательное приготовление говядины являются эффективными в профилактике пищевой передачи инфекции
Важно сообщать о случаях кровавой диареи органам здравоохранения, так как своевременное вмешательство последних может предотвратить возникновение новых случаев инфекции
Обзор
Почечная инфекция – это неприятное и болезненное состояние, которое обычно возникает при попадании бактерий из мочевого пузыря в одну или обе почки. Медицинское название почечной инфекции – пиелонефрит.
В отличие от распространенного заболевания мочевого пузыря- цистита, при котором появляются боли во время мочеиспускания,- это более серьезное состояние.
Несмотря на тяжелое самочувствие, пиелонефрит хорошо поддается лечению на ранних стадиях болезни. Если же почечную инфекцию запустить, болезнь прогрессирует и может привести к необратимому повреждению почек. Обычно симптомы пиелонефрита появляются быстро, в течение нескольких часов. Вы можете почувствовать лихорадку (высокую температуру) и озноб, тошноту, боль в спине или боку.
-
Мочевыводящие пути состоят из:
- почек, которые выделяют из крови отходы жизнедеятельности и превращают их в мочу;
- мочеточников – трубок, соединяющих почки с мочевым пузырем;
- мочевого пузыря – органа, в котором скапливается моча;
- уретры – трубки, через которую моча выводится из организма.
Почки – это два бобовидных органа около 10 см в длину. Они расположены позади брюшной полости по бокам от позвоночника. Почки очищают кровь от ненужных продуктов, которые в виде мочи выводятся из организма. Инфекция, развивающаяся в моче-выделительной системе, называется инфекцией моче-выводящих путей. Так как все части моче-выделительной системы связаны между собой, инфекция легко перемещается с одного органа на соседние и быстро распространяется.
Вам следует обратится к врачу, если у вас высокая температура и постоянная боль в области живота, поясницы или половых органов, а также при нарушении мочеиспускания. В большинстве случаев, при пиелонефрите необходимо скорейшее лечение антибиотиками, чтобы не дать инфекции повредить почки или распространиться в кровь. Вам также могут потребоваться обезболивающие.
Если вы страдаете другими заболеваниями или беременны, то есть более подвержены воздействию инфекции, может понадобиться госпитализация в больницу. Там назначают лечение антибиотиками с помощью капельницы (внутривенного капельного введения).
Как правило, антибиотики являются очень эффективным средством борьбы с пиелонефритом и помогают поправиться уже через две недели. В редких случаях пиелонефрит может вызвать осложнения, в том числе: заражение крови (сепсис) и скопление гноя в почке, так называемый абсцесс.
Как правило, причиной пиелонефрита является кишечная палочка (E. coli). Эта бактерия проникает от ануса (отверстия прямой кишки) в уретру (мочеиспускательный канал, по которому выделяется моча), а затем, через мочевой пузырь – в одну или обе почки.
Пиелонефрит встречается относительно редко. В России, среди взрослых, пиелонефритом в среднем заболевает 1 человек из 877 в год. Он может развиться в любом возрасте. Женщины в 6 раз чаще болеют пиелонефритом, чем мужчины, что связано с особенностями анатомии. Уретра у женщин гораздо короче, чем у мужчин, что облегчает бактериям проникновение в почки. Наиболее подвержены заболеванию молодые женщины, ведущие активную половую жизнь, так как частые половые акты увеличивают риск развития пиелонефрита.
Дети младшего возраста тоже оказывают в группе риска по пиелонефриту, в связи с возможными врожденными нарушениями моче-выделительной системы. Так, частой причиной пиелонефрита у маленьких детей является пузырно-мочеточниковый рефлюкс – противоестественный заброс мочи вверх, от мочевого пузыря в мочеточники и почки.
Эпидемиология ИМП
Инфекции мочевыводящих путей – одно из самых распространенных инфекционных заболеваний человека.
Частота возникновения ИМП зависит от пола и возраста обследуемых, а также от конкретных характеристик исследуемой популяции.
- В неонатальном периоде ИМП выявляется примерно в 60% случаев у мальчиков, что связано с более высокой частотой врожденных дефектов мочевыводящих путей.
- Начиная с трехмесячного возраста, эта тенденция меняется на противоположную, и заболеваемость инфекциями мочевыводящих путей у девочек и женщин в десять раз выше, чем у сверстников-мужчин.
- Каждая вторая женщина хотя бы раз в жизни болеет циститом, а у 10% сексуально активных женщин ИМП развиваются один раз в год.
- Инфекции мочевыводящих путей у мужчин до 50 лет возникают редко, у пациентов старше 60 лет количество зарегистрированных случаев заражения быстро растет. Это связано с появлением непроходимости мочевого пузыря, чаще всего в виде доброкачественной гиперплазии простаты.
- Заболеваемость ИМП намного выше среди людей, госпитализированных по каким-либо причинам, проживающих в интернатах или домах престарелых.
Доброкачественная гиперплазия простаты
Риск ИМП возрастает, когда существует препятствие для оттока мочи или когда обстоятельства способствуют колонизации и росту бактерий. К физиологическим факторам, предрасполагающим к ИМП, относятся беременность, пожилой возраст и такие заболевания, как диабет и мочекаменная болезнь.
Причины ИМВП
Причины инфекции мочевыводящих:
-
Нарушение уродинамики (пузырно-мочеточниковый рефлюкс, обструктивная уропатия, нейрогенная дисфункция мочевого пузыря).
-
Выраженность патогенных свойств микроорганизмов (определенные серотипы, способность кишечной палочки к адгезии на уроэпителии, способность протея выделять уреазу и т.д.).
-
Особенности иммунного ответа пациента (снижение клеточно-опосредованного иммунитета под действием факторов, продуцируемых макрофагами и нейтрофилами, недостаточная продукция антител).
-
Обменные нарушения (сахарный диабет, гиперуратурия, гипероксалатурия, нефрокальциноз, мочекаменная болезнь).
-
Сосудистые изменения в почечной ткани (вазоконстрикция, ишемия).
-
Инструментальные манипуляции на мочевыводящих путях.
Прогноз кишечной инфекции у новорожденного
Кишечная инфекция у новорожденного имеет благоприятные прогнозы в том случае, если заболевание выявлено на ранних стадиях и приняты все необходимые меры для предупреждения обезвоживания и сильной интоксикации организма.
Обезвоживание – одна из основных проблем при кишечной инфекции, так как детский организм быстрее взрослого теряет жидкость и тяжелая дегидратация, особенно при частой рвоте и поносе, может начаться уже в первые часы развития болезни. Такое состояние приводит к нарушению работы мочевыделительной, дыхательной систем, ЦНС, сердца.
Симптомы у новорожденных развиваются очень быстро и главное не упустить момент и вовремя начать действовать и обратиться за квалифицированной помощью, в противном случае, кишечная инфекция может стать причиной смерти малыша.
Кишечная инфекция у новорожденных наиболее распространенное заболевание, так как иммунная система ребенка не сформирована, а устройство пищеварительной системы имеет некоторые особенности. Детский организм вырабатывает меньшее количество соляной кислоты, снижена работа поджелудочной, что облегчает процесс проникновения и развития болезнетворной микрофлоры.
Лечение пиелонефрита
Большинство людей с пиелонефритом могут вылечиться дома с помощью курса антибиотиков и, возможно, обезболивающих препаратов.
Если у вас пиелонефрит, постарайтесь во время мочеиспускания не привставать над унитазом, потому что в таком положении ваш мочевой пузырь может опорожняться не до конца
Также важно употреблять много жидкостей, чтобы избежать обезвоживания и способствовать вымыванию бактерий из ваших почек. Количество выпитой жидкости можно считать достаточным, если вы ходите в туалет чаще обычного, и моча приобрела бледную окраску
Больше отдыхайте. Пиелонефрит может отнимать у вас все силы, даже если обычно вы не жалуетесь на здоровье. Для того, чтобы полностью поправиться и вернуться на работу, может потребоваться до двух недель.
Если вы лечитесь на дому, скорее всего, вам пропишут курс антибиотиков в виде таблеток или капсул, которые необходимо принимать от одной до двух недель. Существует большое количество антибиотиков, которые используются для лечения инфекций почек. Но только врач может подобрать наиболее эффективный из них в вашем случае.
К распространенным побочным эффектам антибиотиков относится тошнота и понос. Некоторые из антибактериальных препаратов могут снижать эффективность пероральных контрацептивов и контрацептивных пластырей, поэтому на время лечения, вам могут понадобиться другие противозачаточные средства.
Беременным женщинам при развитии пиелонефрита тоже необходим прием антибиотиков. Выбор лекарственного препарата основывается на его эффективности против бактерий, вызвавших почечную инфекцию, и безопасности для плода. Антибиотик и режим его приема должен назначать только врач. Вам должно стать лучше вскоре после начала лечения, и вы должны полностью поправиться примерно через 2 недели. Если спустя 48-72 часа от начала лечения состояние не улучшается, обратитесь к лечащему врачу.
Обезболивающие, такие как парацетамол, должны облегчить боль и снизить температуру. Однако, нестероидные противовоспалительные средства (НПВС), такие как ибупрофен, для этих целей принимать не рекомендуется. Эти препараты могут ухудшить состояние почек при пиелонефрите.
Терапевт может направить вас к узкому специалисту – урологу, если считает, что у вас есть какая-то причина, которая повышает вероятность развития почечных инфекций. Уролог – это хирург, специализирующийся на лечении заболеваний моче-выводящих путей. Обычно, для дополнительного обследования к урологу направляют всех мужчин с пиелонефритом, так как у них это заболевание встречается реже, чем у женщин. Среди женщин к урологу обычно направляют лишь тех, у кого было два или более случаев пиелонефрита.
Дети, страдающие пиелонефритом, должны пройти осмотр у врача, специализирующегося на детских болезнях.
Когда нужна госпитализация при пиелонефрите
В некоторых случаях лечение должно проводиться в больнице, а не на дому. Необходимо лечь в больницу, если:
- вы сильно обезвожены;
- вы не можете глотать или все лекарства и жидкости удаляются с рвотой;
- у вас есть дополнительные симптомы, указывающие на вероятность заражения крови, например, учащенное сердцебиение или потеря сознания;
- вы беременны, и у вас высокая температура;
- ваш организм особенно ослаблен, у вас общее тяжелое состояние;
- нет улучшения через 48 часов от начала лечения антибиотиками;
- у вас ослабленный иммунитет;
- у вас в моче-выводящих путях есть инородное тело, например, почечный камень или мочевой катетер;
- у вас диабет;
- вам больше 65 лет;
- у вас есть заболевание, влияющее на работу моче-выделительных органов, например, поликистоз почек или другое хроническое заболевание почек.
Большинство детей с пиелонефритом будут проходить лечение в больнице.
Если вас положили в больницу с пиелонефритом, скорее всего, вам поставят капельницу, чтобы ваше тело получало достаточное количество жидкости. Антибиотики также могут подаваться через капельницу. У вас будут регулярно брать кровь и мочу на анализ, чтобы следить за состоянием вашего здоровья и за тем, насколько эффективно антибиотики борются с инфекцией.
Как лечится эшерихиоз?
Эшерихиоз лечится эмпирическим путем, а впоследствии лечение модифицировано согласно результатам исследования на чувствительность к антибиотикам. Многие штаммы кишечной палочки резистентны к пенициллину и тетрациклинам, поэтому необходимо использовать другие антибиотики, включая тикарциллин, пиперациллин, цефалоспорины, аминогликозиды, триметоприм-сульфаметоксазол и фторхинолоны. Для дренирования гноя, очищения очагов некротического повреждения и удаления инородных тел может потребоваться хирургическое вмешательство.
В основном лечение при данной инфекции — поддерживающее. Несмотря на то что кишечная палочка чувствительна к наиболее часто используемым антимикробным препаратам, антибиотики не влияют на эволюцию симптомов, устранение носительства или профилактику гемолитико-уремического синдрома. К тому же есть подозрение, что фторхинолоны способствуют выделению энтеротоксина.
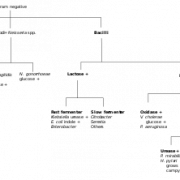
Эпидемиология
Е. coli является представителем нормальной микрофлоры кишечного тракта всех млекопитающих, птиц, рептилий и рыб. Поэтому для выяснения вопроса, какие варианты Е. coli и почему вызывают эшерихиозы, потребовалось изучить антигенное строение, разработать серологическую классификацию, необходимую для идентификации патогенных серовариантов, и выяснить, какими факторами патогенности они обладают, т. е. почему они способны вызывать различные формы эшерихиозов.
У Е. coli обнаружен 171 вариант О-антигенов (01-0171), 57 вариантов Н-антигенов (H1-H57) и 90 вариантов поверхностных (капсульных) К-антигенов. Однако в действительности существует 164 группы по О-антигену и 55 серовариантов по Н-антигену, так как некоторые из прежних 0:Н-серогрупп были исключены из вида E. coli, но порядковые номера О- и Н-антигенов сохранились неизменными. Антигенная характеристика диареегенных Е.соli включает в себя номера О- и Н-антигенов, например, 055:116; 0157:Н7; О-антиген означает принадлежность к определенной серогруппе, а Н-антиген — ее серовариант. Кроме того, при более углубленном изучении О- и Н-антигенов выявлены так называемые факторные О- и Н-антигены, т. е. их антигенные субварианты, например: Н2а, Н2Ь, Н2с или 020, О20а, O20ab и т. п. Всего в список диареегенных Е. coli включено 43 О-серогруппы и 57 ОН-серовариантов. Список этот пополняется все новыми серовариантами.
Экология
Резервуаром Кишечной палочки в природе является человек, толстая кишка к-рого заселяется разными биотипами этого микроба с момента перехода ребенка на смешанное питание, примерно к концу первого года жизни. Количество К. п. в 1 г испражнений колеблется от нескольких миллионов до 1—3 млрд. особей. На протяжении жизни человека происходит многократная смена биотипов К. п. в кишечнике. Определенную роль в этом процессе играет режим питания, перенесенные инфекции, лечение химиопрепаратами, антибиотиками и другие факторы. В естественных условиях К. п. обитает также в кишечнике домашних животных, птиц, диких млекопитающих, рептилий, рыб и многих беспозвоночных.
Особенности применения пробиотиков и пребиотиков у детей
Препараты из группы пробиотиков и пребиотиков очень часто назначаются детям разного возраста с лечебно-профилактической целью. Препараты, сочетающие в себе пробиотический и пребиотический компоненты, являются незаменимой составляющие комплексной терапии инфекционного и неинфекционного гастроэнтерита, энтерита и кишечного дисбиоза в периоде новорожденности. Для восстановления микрофлоры после антибиотиков, ребенку назначают пробиотики и пребиотики с первого дня начала антибактериального лечения.
С точки зрения эффективности, комбинированный прием антибиотиков и пробиотиков малоэффективен, так как от общего количества принимаемых бактерий, жизнеспособными остаются не более 25%. Решить эту проблему позволило изобретение метапребиотика, который содержит комбинацию из фруктоолигосахаридов и фруктополисахаридов, а также лактат кальция. Метапребиотик Стимбифид Плюс для детей не нормализует кишечную микрофлору за счёт содержания бифидум и лактобактерий, но при попадании в просвет желудочно-кишечного тракта, компоненты Стимбифид Плюс создают максимально благоприятные условия для размножения нормальной микрофлоры.
При контакте с антибиотиками, эффективность метапребиотика не снижается, поэтому Стимбифид для детей одинаково совместим с любыми антибактериальными препаратами. Восстанавливая нормальную микробиоту желудка и кишечника, Стимбифид Плюс повышает иммунитет и помогает гармонизировать все процессы в организме ребенка. Компоненты метапребиотика благоприятно влияют на интеллектуальное развитие детей, и помогают улучшить школьную успеваемость. Метапребиотик для детей полностью безопасен, поэтому может быть использован с лечебно-профилактической целью уже с первых дней жизни. В инструкции по применению Симбифид Плюс, для детей обозначена дозировка и кратность приёма.
18.05.2020
7765
14
/ Доктор Стимбифид
Как лечатся мочевыводящие инфекции у новорожденных
У новорожденных детей антибиотик вводится парентерально, у большинства остальных детей орально. В случае чувствительности к препарату моча становится стерильной через 24 часа после начала лечения. При сохранении бактерий в моче во время лечения говорит о резистентности возбудителя к препарату. Другие симптомы воспаления сохраняются дольше, повышение температуры до 2-3 дней, лейкоцитурия до 3-4 дней, повышение СОЭ может наблюдаться до 3 недель. Длительность лечения антибиотиками в среднем составляет 10 дней.
У детей с циститом задачей лечения является освобождение от дизурии, которая у большинства проходит в течение 1-2 дней, поэтому прием антибиотика в течение 3-5 дней оказывается обычно достаточным. У детей с пиелонефритом необходимо предупредить персистенцию инфекции и сморщивание почки. У пациентов с высоким риском прогрессирования профилактика должна проводиться в течение нескольких лет. При проведении лечения необходимо проводить с родителями разъяснительную работу о необходимости профилактических курсов лечения, на возможный неблагоприятный прогноз при наличии факторов прогрессирования.
1. И.Е.Тареева. Нефрология. Руководство для врачей Медицина 2000 г.
2. Т.В. Сергеева, О.В. Комарова. Инфекция мочевыводящих путей. Вопросы современной педиатрии 2002 г.
Автор статьи врач-педиатр Гончарова М.В.
Источник Сибирский медицинский портал